Sanofi et sa filiale Genzyme ont annoncé les premiers résultats, "positifs", de la première étude de phase 3 du médicament Lemtrada (alemtuzumab, Campath) pour le traitement de la sclérose en plaques.
Au cours des 2 ans qu'a duré cet essai clinique, mené avec 581 personnes atteintes de la forme cyclique (poussées-rémissions) de la maladie, une réduction de 55 % du taux de poussées par rapport à Rebif (Interferon beta-1a) du laboratoire allemand Merck KGaA, un traitement actuel de référence, a été constatée.
Mais le délai écoulé jusqu'à une accumulation durable du handicap pendant six mois n'était pas significativement différent du délai obtenu avec Rebif, ce qui a entraîné une baisse des actions de Sanofi, le plus important laboratoire français, après cette annonce.
Les effets secondaires étaient notamment des maux de têtes, la fièvre, les nausées, les démangeaisons, les frissons et une augmentation des infections (dont les plus fréquentes étaient respiratoires et urinaires ainsi que l'herpès oral).
L'alemtuzumab est un anticorps utilisé pour le traitement d'une forme de leucémie.
Sanofi entend déposer des demandes d'autorisation de mise sur le marché aux États-Unis et dans l'Union européenne au début de 2012.
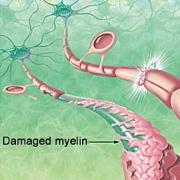
Illustration : Dans la sclérose en plaques, la gaine myéline protégeant les fibres nerveuses est endommagée, ce qui nuit à la transmission de l'influx nerveux.
-
Psychomédia avec sources:
Tous droits réservés










