Le laboratoire suisse Roche a annoncé vendredi les résultats d'une étude randomisée de phase III (dernière avant les demandes d'autorisation de mise sur le marché) concernant son médicament trastuzumab emtansine (T-DM1, Kadcyla) destiné au traitement du cancer du sein HER2-positif (récepteurs HER2 à la surface des cellules cancéreuses; 15% à 25% des cancers du sein).
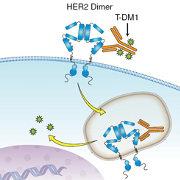
Ce médicament, un conjugué anticorps-médicament, composé du trastuzumab (Herceptin), un anticorps monoclonal qui cible les récepteurs HER2, et du DM1, un agent de chimiothérapie.
Il vise à cibler et inhiber la voie de signalisation du HER2 (bloquer des signaux permettant à la tumeur de croître) et délivrer l'agent chimiothérapique DM1 directement à l'intérieur des cellules cancéreuses HER2-positives.
L'étude a été menée avec des femmes atteintes d'un cancer du sein métastatique HER2-positif ayant déjà reçu un traitement par Herceptin et une chimiothérapie. Les femmes traitées par le trastuzumab emtansine "ont vécu significativement plus longtemps sans aggravation de la maladie
" que les femmes traitées par lapatinib en combinaison avec le Xeloda (capécitabine).
Les résultats finaux concernant la survie globale ne sont pas encore disponibles. Le profil d'innocuité du trastuzumab emtansine correspondait à ceux observés lors de précédentes études.
Roche prévoit déposer cette année une demande d’autorisation de mise sur le marché (AMM) à l’Agence européenne des médicaments (EMA) et, aux États-Unis, sa filiale Genentech fera de même auprès de la Food and Drug Administration (FDA).
Un anticorps monoclonal de Roche, l'Avastin (bévacizumab), a perdu en novembre dernier son approbation pour le traitement des cancers du sein avec métastases aux États-Unis en raison d'une absence de preuve de son efficacité et d'effets secondaires graves. Il demeure approuvé pour d'autres cancers.
Psychomédia avec source: Doctissimo, Boursier, Le Figaro.
Tous droits réservés.










